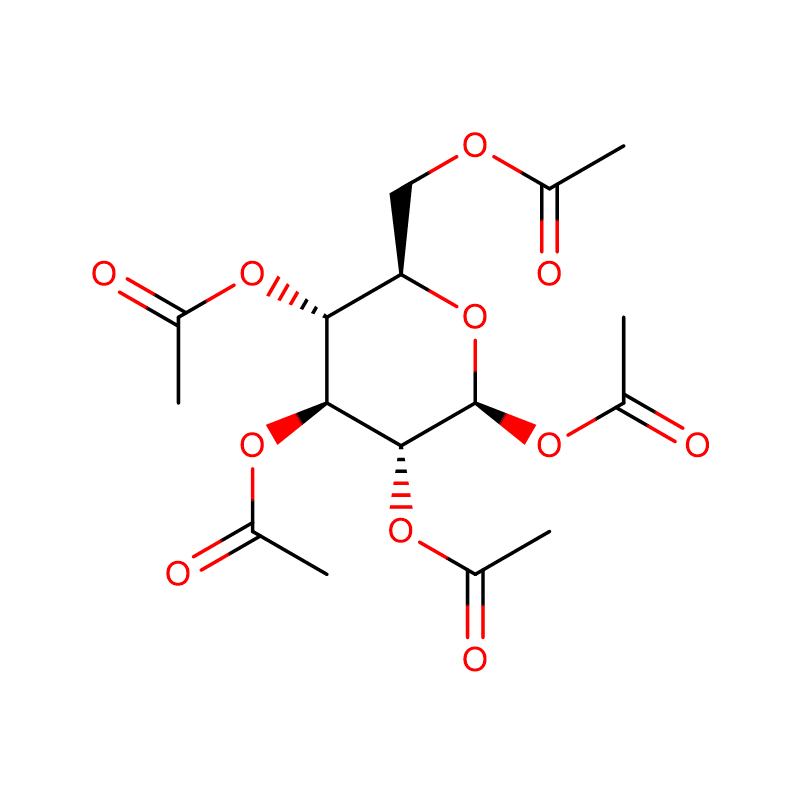
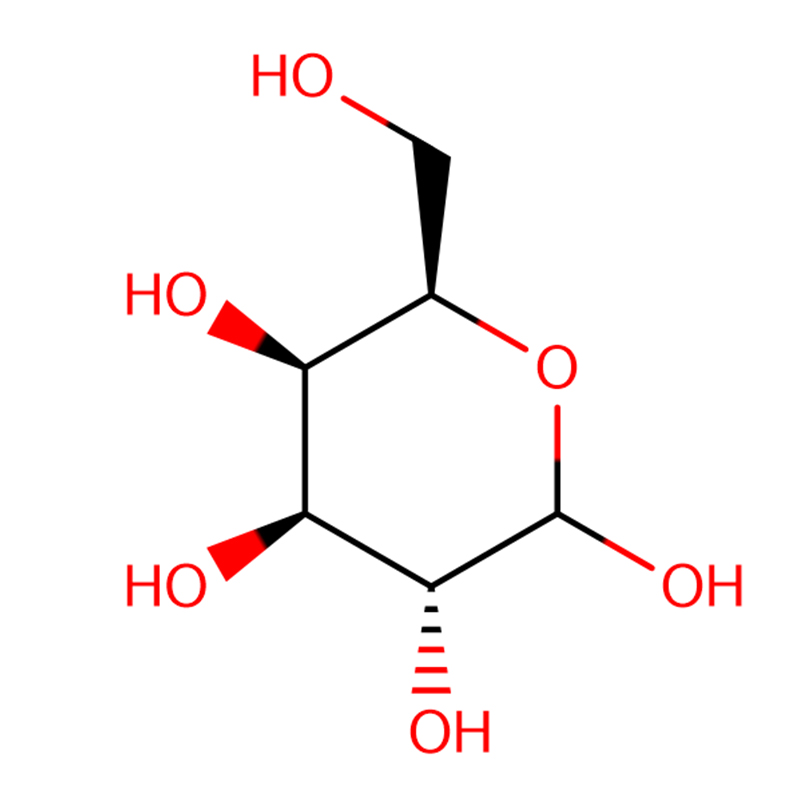
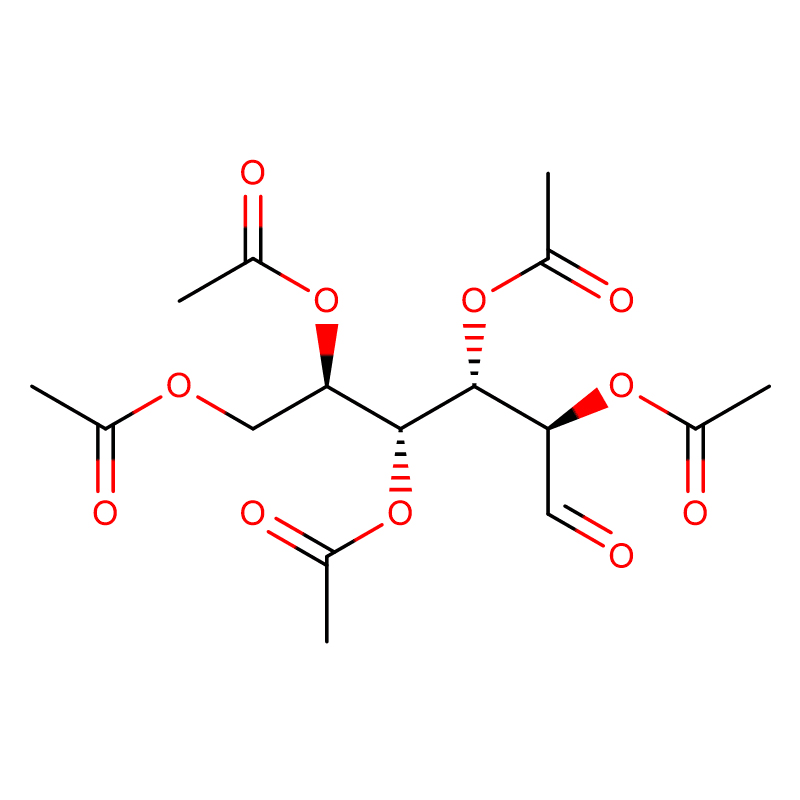
4-NITROPHENYL-ALPHA-D-MANNOPYRANOSIDE CAS: 10357-27-4 Polvere bianca 98%
| Numeru di catalogu | XD90011 |
| Nome di u produttu | 4-Nitrofenil-alfa-D-mannopiranoside |
| CAS | 10357-27-4 |
| Formula Molecular | C12H15NO8 |
| Pesu Molecular | 30301.25 |
| Dettagli di almacenamentu | -2à -8°C |
| Codice Tariffa Armonizatu | 29400000 |
Specificazione di u produttu
| Acqua | <5% Karl Fische |
| Solubilità | 1% in DMF hè chjaru è incolore |
| Purità | 4-Nitrofenolu liberu <200 ppm |
| HPLC | > 98% |
| Apparizione | Polvere bianca |
Insights meccanicisti in una famiglia dipendente da Ca2+ di alfa-mannosidasi in un simbionte intestinale umanu.
I batteri colonichi, esemplificati da Bacteroides thetaiotaomicron, ghjucanu un rolu chjave in u mantenimentu di a salute umana sfruttendu grandi famiglie di glycoside hydrolases (GHs) per sfruttà i polisaccaridi dietetichi è i glicani d'ospiti cum'è nutrienti.Tali espansione di a famiglia GH hè exemplificata da a famiglia 23 GH92 glycosidases codificata da u genoma B. thetaiotaomicron.Quì mostramu chì si tratta di l'alfa-mannosidasi chì agiscenu per via di un unicu mecanismu di spustamentu per utilizà l'ospiti N-glicani.A struttura tridimensionale di dui mannosidasi GH92 definisce una famiglia di proteine du duminii in quale u centru cataliticu hè situatu à l'interfaccia di u duminiu, chì furnisce assistenza à l'acidu (glutamate) è basa (aspartate) à l'idrolisi in un Ca(2+)- manera dipendente.E strutture tridimensionali di u GH92s in cumplessu cù inhibitori furniscenu una visione di a specificità, u mekanismu è l'itinerariu conformazionale di a catalisi.Ca(2+) ghjoca un rolu cataliticu chjave per aiutà à distorsioni u mannoside luntanu da a so conformazione di sedia (4)C (1) in u statu di terra versu u statu di transizione.(Bibliografia: Nat.Chem.Biol.6, 125-32, (2010)
Cromatografia di affinità frontale di ovalbumin glycoasparagines nantu à una colonna di concanavalin A-sepharose.Un studiu quantitatiu di a specificità di u ligame di a lectina.
L'interazzione di a concanavalina A (ConA) immobilizzata da Sepharose 4B cù 10 glicoasparagine derivate da l'ovalbumina sò state investigate quantitativamente da cromatografia di affinità frontale.In questu metudu, una suluzione di carbuidrati hè appiicata continuamente à una colonna ConA-Sepharose è a ritardazione di u fronte di l'eluzione hè misurata cum'è un paràmetru di a forza di l'interazzione.A constante di dissociazione (Kd) per ogni saccharide cun ConA pò esse determinata.Un analisi di u ligame di p-nitrophenyl-alpha,D-mannoside hà dimustratu chì e proprietà di ubligatoriu di ConA ùn cambianu micca essenzialmente dopu l'immobilizazione nantu à Sepharose 4B.Ciascuna di l'ovalbumin glycoasparagines hè stata marcata cù tritium da u metudu di metilazione riduttiva per l'analisi.Un paragone di i valori di Kd ottenuti hà dimustratu chì u ligame di ConA varia considerablemente cù differenze strutturali assai ligeri di a catena glicosilica.I risultati suggerenu chì ConA ricunnosce una struttura specifica di a catena glycosyl, Man alpha 1-6 (Man alpha 1-3) Man, in quale almenu un gruppu hydroxyl à a pusizione C-3 di mannose C-6-linked deve esse liberu.